Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir?
Alüminyum hidrit Nedir?
Alüminyum hidrit Nedir?, Alüminyum hidrit Nerededir?, Alüminyum hidrit Hakkında Bilgi?, Alüminyum hidrit Analizi? Alüminyum hidrit ilgili Alüminyum hidrit ile ilgili bilgileri sitemizde bulabilirsiniz. Alüminyum hidrit ile ilgili daha detaylı bilgi almak ve iletişime geçmek için sayfamıza tıklayabilirsiniz. Alüminyum hidrit Ne Anlama Gelir Alüminyum hidrit Anlamı Alüminyum hidrit Nedir Alüminyum hidrit Ne Anlam Taşır Alüminyum hidrit Neye İşarettir Alüminyum hidrit Tabiri Alüminyum hidrit Yorumu
Alüminyum hidrit Kelimesi
Lütfen Alüminyum hidrit Kelimesi İle ilgili Daha Fazla Bilgi Almak İçin Kategoriler Sayfamıza Bakınız. Alüminyum hidrit İlgili Sözlük Kelimeler Listesi Alüminyum hidrit Kelimesinin Anlamı? Alüminyum hidrit Ne Demek? ,Alüminyum hidrit Ne Demektir? Alüminyum hidrit Ne Demektir? Alüminyum hidrit Analizi? , Alüminyum hidrit Anlamı Nedir?,Alüminyum hidrit Ne Demektir? , Alüminyum hidrit Açıklaması Nedir? ,Alüminyum hidrit Cevabı Nedir?,Alüminyum hidrit Kelimesinin Anlamı?,Alüminyum hidrit Kelimesinin Anlamı Nedir? ,Alüminyum hidrit Kelimesinin Anlamı Ne demek?,Alüminyum hidrit Kelimesinin Anlamı Ne demektir?
Alüminyum hidrit Bu Kelimeyi Kediniz Aradınız Ve Bulamadınız
Alüminyum hidrit Kelimesinin Anlamı Nedir? Alüminyum hidrit Kelimesinin Anlamı Ne demek? , Alüminyum hidrit Kelimesinin Anlamı Ne demektir?
Demek Ne Demek, Nedir? Tdk'ye Göre Anlamı
Demek kelimesi, dilimizde oldukça kullanılan kelimelerden birisidir. TDK'ye göre, demek kelimesi anlamı şu şekildedir:
Söylemek, söz söylemek - Ad vermek - Bir dilde karşılığı olmak - Herhangi bir ses çıkarmak - Herhangi bir kanıya, yargıya varmak - Düşünmek - Oranlamak - Ummak, - Erişmek - Bir işe kalkışmak, yeltenmek - Saymak, kabul etmek - bir şey anlamına gelmek - öyle mi, - yani, anlaşılan - inanılmayan, beklenmeyen durumlarda kullanılan pekiştirme veya şaşma sözü
Alüminyum hidrit Bu Kelimeyi Kediniz Aradınız Ve Bulamadığınız İçin Boş Safyadır
Demek Kelimesi Cümle İçerisinde Kullanımı
Eskilerin dediği gibi beşer, şaşar. - Muşmulaya döngel de derler.
Kamer `ay` demektir. - Küt dedi, düştü. - Bu işe herkes ne der? - Güzellik desen onda, zenginlik desen onda. - Bundan sonra gelir mi dersin? - Saat yedi dedi mi uyanırım. - Kımıldanayım deme, kurşunu yersin. Ağzını açayım deme, çok fena olursun. - Yarım milyon dediğin nedir? - Okuryazar olmak adam olmak demek değildir. - Vay! Beni kovuyorsun demek, pekâlâ! Alüminyum hidrit - Demek gideceksin.
Demek Kelimesi Kullanılan Atasözü Ve Deyimler
- dediği çıkmak - dediğinden (dışarı) çıkmak - dediğine gelmek
- dedi mi - deme! - demediğini bırakmamak (veya koymamak) - deme gitsin - demek istemek , - demek ki (veya demek oluyor ki) , - demek olmak , - dememek - der oğlu der - deyip de geçmemek - diyecek yok - dediği çıkmak , {buraya- - dediğinden (dışarı) çıkmak - dediğine gelmek i, - dedi mi , {buraya- - deme! - demediğini bırakmamak (veya koymamak) - deme gitsin , - demek istemek - demek ki (veya demek oluyor ki) - demek olmak - dememek - der oğlu der - deyip de geçmemek - diyecek yok
Alüminyum hidrit
Alüminyum hidrit Nedir? Alüminyum hidrit Ne demek? , Alüminyum hidrit Kelimesi İle ilgili Daha Fazla Bilgi , Almak İçin Kategoriler Sayfamıza Bakınız. İlgili Sözlük Kelimeler Listesi
Alüminyum hidrit Kelimesinin Anlamı? Alüminyum hidrit Ne Demek? Alüminyum hidrit Ne Demektir? ,Alüminyum hidrit Analizi? Alüminyum hidrit Anlamı Nedir? Alüminyum hidrit Ne Demektir?, Alüminyum hidrit Açıklaması Nedir? , Alüminyum hidrit Cevabı Nedir? , Alüminyum hidrit Kelimesinin Anlamı?
Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir?
Alüminyum hidrür
Bu madde veya sayfa en dilinden dilinden kötü bir biçimde tercüme edilmiştir. Sayfa makine çevirisi veya dilde yetkinliği bulunmayan bir çevirmen tarafından oluşturulmuş olabilir. (Ocak 2024) |

| |
| Adlandırmalar | |
|---|---|
Alüminyum hidrür | |
Alüman | |
Diğer adlar Alan Alüminik hidrür | |
| Tanımlayıcılar | |
3D model (JSmol)
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.029.139 |
| 245 | |
PubChem CID
|
|
CompTox Bilgi Panosu (EPA)
|
|
| |
| |
| Özellikler | |
| Molekül formülü | AlH3 |
| Molekül kütlesi | 29,99 g/mol |
| Görünüm | beyaz kristal katı, uçucu olmayan, çok polimerleşmiş, iğne benzeri kristaller |
| Yoğunluk | 1,477 g/cm3, katı |
| Erime noktası | 150 °C |
| Çözünürlük (su içinde) | tepkir |
| Termokimya | |
Isı sığası (C)
|
40,2 J/mol K |
Standart molar entropi (S⦵298)
|
30 K/mol K |
Standart formasyon entalpisi (ΔfH⦵298)
|
-11,4 kJ/mol |
Gibbs serbest enerjisi (ΔfG⦵)
|
46,4 kJ/mol |
| Benzeyen bileşikler | |
Benzeyen bileşikler
|
Lityum alüminyum hidrür, diboran |
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |
| Bilgi kutusu kaynakları | |
Alüminyum hidrür (ayrıca bilinen adıyla alan veya alüman), formülü AlH3 olan inorganik bileşik. Renksiz, piroforik ve katı bir maddedir. Araştırma laboratuvarlarının dışında nadiren karşılaşılmasına rağmen, alan ve türevleri organik sentezlerde indirgen madde olarak kullanılır.[1]
Yapısı[değiştir | kaynağı değiştir]
Alan, bir polimerdir. Bu nedenle, bileşiğin formülü bazen (AlH3)n formülü ile gösterilir. α-alan, α’-alan, β-alan, γ-alan, δ-alan, ε-alan and ζ-alan diye adlandırılan sayısız polimorflardan oluşur. α-Alan, kübik veya karbohedral morfolojiye sahiptir. Buna karşılık α’-alan, iğne benzeri kristallerden oluşurken; γ-alan, erimiş iğne demetlerinden oluşur. Alan, THF ve eterde çözünür. Katı alanın eterde çökelme oranı hazırlama yöntemine göre değişir.[2]
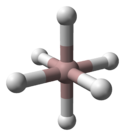
α-alanın kristal yapısı kararlıdır ve 6 alüminyum atomuyla köprü oluşturan, 6 hidrojen atomuyla çevrili alüminyum atomlarını içerir. Al-H uzaklıklarının tümü eş değere (172pm) sahiptir. Al-H-Al açısı 141°dir.[3]
 |
 |
 |
α-Alan, sıklıkla termal olarak kararlı bir polimorftur. β-alan ve γ-alan, beraber üretilir ve ısıtılarak α-alana dönüşür. δ, ε ve θ-alan, diğer kristalleşme koşullarında üretilir. Termal olarak daha kararlı olmasına rağmen δ, ε ve θ polimorfları ısıtmayla α-alana dönüşmez.[2]
Alanın moleküler şekilleri[değiştir | kaynağı değiştir]
Düzlemsel olarak gösterilen monomerik AlH3, katı bir soy gaz matrisinde düşük sıcaklıkta izole edilmiştir.[4] Dimerik Al2H6, katı hidrojen içinde izole edilmiştir. Diboran (B2H6) ve digallan (Ga2H6) ile eş yapıdadır.[5][6]
Hazırlanışı[değiştir | kaynağı değiştir]
Alüminyum hidrürler ve bunların çeşitli kompleksleri uzun zamandır bilinmektedir.[7] İlk sentezi 1947 yılında yapıldı ve 1999 yılında sentez için bir patent alındı.[8][9] Alüminyum hidrit, alüminyum klorür ile lityum alüminyum hidrürün kimyasal işleme tutulmasıyla hazırlanır.[10] Karmaşık olan bu işlemde, lityum klorür'ün çıkarılmasında dikkatli olunmalıdır.
- 3 LiAlH4 + AlCl3 → 4 AlH3 + 3 LiCl
Katı hâldeki madde hızla çöktüğünden, eter çözeltisinin derhal kullanılması gerekir. Alüminyum hidrür çözeltisinin 3 gün sonra yükseltgendiği bilinmektedir. Alüminyum hidrür, LiAlH4 bileşiğinden daha reaktiftir.[2]
Alüminyum hidrürün hazırlandığı diğer yöntemler aşağıdaki gibidir:
- 2 LiAlH4 + BeCl2 → 2 AlH3 + Li2BeH2Cl2
- 2 LiAlH4 + H2SO4 → 2 AlH3 + Li2SO4 + 2 H2
- 2 LiAlH4 + ZnCl2 → 2 AlH3 + 2 LiCl + ZnH2
Elektrokimyasal sentez[değiştir | kaynağı değiştir]
Birkaç grup, alüminyum hidrürün elektrokimyasal olarak üretilebildiğini göstermiştir.[11][12][13][14][15] Alüminyum hidrürün elektrokimyasal olarak üretilen farklı yöntemlerinin patenti alınmıştır.[16][17] Elektrokimyasal olarak üretilen alüminyum hidrür, klorür yabancı maddelerini önler. Clasen'in çözücü olarak THF'yi, elektrolit olarak sodyum alüminyum hidrür, bir alüminyum anodu ve katot olarak cıvaya (Hg) batırılmış bir demir (Fe) telini içeren elektrokimyasal hücresinde oluşumu için iki olası mekanizma tartışılmaktadır. Sodyum, HG katotu ile yan reaksiyonları önleyen bir amalgam oluşturur. İlk reaksiyonda üretilen hidrojen yakalanabilir ve sodyum hidrit üretmek için sodyum cıva amalgamı ile geri tepkimeye sokulabilir. Clasen'in sisteminde başlangıç malzemesi kaybolmaz. Çözülmeyen bir anot için 1. reaksiyona bakın.
1. AlH4− - e− → AlH3 · nTHF + ½H2 Çözünebilen anotlar için, 2. reaksiyona göre anodik çözünme beklenir,
2. 3AlH4− + Al - 3e− → 4AlH3 · nTHF 2. reaksiyonda alüminyum anotu tüketilir, belirli bir elektrokimyasal hücre için alüminyum hidrür üretimini sınırlar.
Alüminyum hidrürün elektrokimyasal olarak üretilen alan'dan kristalleşmesi ve geri kazanımı gösterilmiştir.[14][15]
Alüminyum metalinin yüksek basınçlı hidrojenasyonu[değiştir | kaynağı değiştir]
α-AlH3, 10GPa ve 600 °C (1.112 °F) koşullarında alüminyum metalinin hidrojenasyonuyla üretilebilir. Sıvılaştırılmış hidrojen arasındaki reaksiyon, ortam koşullarında geri kazanılabilen α-AlH3 üretir.[18]
Reaksiyonları[değiştir | kaynağı değiştir]
Lewis bazlarıyla eklenme ürünlerinin oluşumu[değiştir | kaynağı değiştir]
AlH3, kolaylıkla Lewis bazlarıyla eklenme ürünü oluşturur. Örneğin trimetilamin ile 1:1 ve 1:2 kompleksleri oluşturur. 1:1 kompleksi, gaz fazında dört yüzlü,[19] ama katı fazda, köprü oluşturan hidrojen merkezleri (NMe3Al(μ-H))2 ile dimerik olur.[20] 1:2 kompleksi, trigonal bipiramidal bir yapıya sahiptir.[19] Bazı eklenme ürünleri (Örn; dimetiletilamin alan, NMe2Et · AlH3), alüminyum metali vermek için termal olarak ayrışır ve böylelikle MOCVD uygulamalarında kullanılabilir.[21]
Dietil eter ile kompleksi aşağıdaki tamkatlamaya göre oluşur:
- AlH3 + (C2H5)2O → H3Al · O(C2H5)2
Eter içindeki lityum hidrür ile reaksiyonu, lityum alüminyum hidrür üretir:
- AlH3 + LiH → LiAlH4
Fonksiyonel grupların indirgenmesi[değiştir | kaynağı değiştir]
Organik kimyada alüminyum hidrür, ağırlıklı olarak fonksiyonel grupların indirgenmesinde kullanılır.[22] Birçok yoldan alüminyum hidrürün reaktifliği, lityum alüminyum hidrür bileşiğine benzer. Alüminyum hidrür; aldehitler, ketonlar, karboksilik asitler, anhidritler, açil klorürler, esterler ve laktonları kendi alkollerine indirger. Amidler, nitriller ve oksimler aminlere indirgenir.
Fonksiyonel grup seçiciliği açısından alan, diğer hidrür reaktiflerinden farklıdır. Buna örnek olarak; aşağıdaki siklohekzanon indirgenmesinde lityum alüminyum hidrür, 1.9 : 1 oranında trans:cis verirken alüminyum hidrür, 7.3 : 1 oranında trans:cis verir.[23]

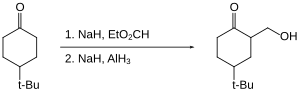
Alan, bazı ketonların hidroksimetilasyonunu, yani C-H'nin C-CH2OH ile yer değiştirmesini sağlar.[24] Keton, enolat olarak "korunduğu" için indirgenmez.
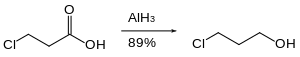
Halokarbonlar, alüminyum hidrür ile yavaşça indirgenir veya hiç indirgenmez. Bu nedenle karboksilik asitler gibi reaktif fonksiyonel gruplar, halojenürlerin varlığında indirgenebilirler.[25]
Azor grupları, alüminyum hidrür ile indirgenmez. Benzer şekilde alüminyum hidrür, azot gruplarının varlığında esterin indirgenmesini sağlayabilir.[26]

Alüminyum hidrür, asetallerin yarı korunmuş diollere indirgenmesinde kullanılabilir.[27]

Alüminyum hidrür, ayrıca aşağıda gösterildiği gibi epoksit halka açma reaksiyonunda da kullanılabilir.[28]

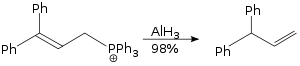
Alüminyum hidrür kullanılarak gerçekleştirilen allilik yeniden düzenlenme reaksiyonu, bir SN2 reaksiyonudur ve sterik olarak talep edilmemektedir.[29]
Alüminyum hidrüf, metan vermek için karbondioksiti de indirger.
- 4 AlH3 + 3 CO2 → 3 CH4 + 2 Al2O3
Hidroalüminasyon[değiştir | kaynağı değiştir]
Alüminyum hidrürün propargil alkollere eklendiği gösterilmiştir.[30] Hidroborasyon benzeri bir reaksiyon olarak, titanyum tetraklorür ile birlikte kullanıldığında çift bağlara katlanabilir.[31]

Yakıt[değiştir | kaynağı değiştir]
Alüminyum hidrür, hidrojen yakıtlı araçlarda hidrojenin depolanması için tartışılmıştır. 148g/L'ye karşılık gelen AlH3, ağırlıkça %10'a kadar hidrojen içerir ve H2 sıvısının iki katıdır. Ancak, AlH3 geri dönüşümlü bir hidrojen taşıyıcısı değildir.[32] Patlayıcı ve piroteknik bileşimlerde roket yakıtına potansiyel bir katkıdır.
Önlemler[değiştir | kaynağı değiştir]
Alüminyum hidrür kendiliğinden yanıcı değildir, ama lityum alüminyum hidrüre benzer şekilde oldukça reaktiftir. Hava ve suda parçalanır. Her ikisinde de şiddetli reaksiyonlar oluşur.[2] AlH3, alüminyum oksitin koruyucu tabakasıyla havada dikkatle, güvenli bir şekilde ele alınabilir.[32]
Kaynakça[değiştir | kaynağı değiştir]
- ^ Brown, H. C.; Krishnamurthy, S. (1979). "Forty Years of Hydride Reductions". Tetrahedron. 35 (5). ss. 567-607. doi:10.1016/0040-4020(79)87003-9.
- ^ a b c d US application 2007066839 2 Şubat 2019 tarihinde Wayback Machine sitesinde arşivlendi., Lund, G. K.; Hanks, J. M.; Johnston, H. E., "Method for the Production of α-Alane"
- ^ Turley, J. W.; Rinn, H. W. (1969). "The Crystal Structure of Aluminum Hydride". Inorganic Chemistry. 8 (1). ss. 18-22. doi:10.1021/ic50071a005.
- ^ Kurth, F. A.; Eberlein, R. A.; Schnöckel, H.-G.; Downs, A. J.; Pulham, C. R. (1993). "Molecular Aluminium Trihydride, AlH3: Generation in a Solid Noble Gas Matrix and Characterisation by its Infrared Spectrum and ab initio Calculations". Journal of the Chemical Society, Chemical Communications. 1993 (16). ss. 1302-1304. doi:10.1039/C39930001302.
- ^ Andrews, L.; Wang, X. (2003). "The Infrared Spectrum of Al2H6 in Solid Hydrogen". Science. 299 (5615). ss. 2049-2052. Bibcode:2003Sci...299.2049A. doi:10.1126/science.1082456. PMID 12663923.
- ^ Pulham, C. R.; Downs, A. J.; Goode, M. J.; Rankin D. W. H.; Robertson, H. E. (1991). "Gallane: Synthesis, Physical and Chemical Properties, and Structure of the Gaseous Molecule Ga2H6 as Determined by Electron Diffraction". Journal of the American Chemical Society. 113 (14). ss. 5149-5162. doi:10.1021/ja00014a003.
- ^ Brower, F. M.; Matzek, N. E.; Reigler, P. F.; Rinn, H. W.; Roberts, C. B.; Schmidt, D. L.; Snover, J. A.; Terada, K. (1976). "Preparation and Properties of Aluminum Hydride". Journal of the American Chemical Society. 98 (9). ss. 2450-2454. doi:10.1021/ja00425a011.
- ^ Finholt, A. E.; Bond, A. C. Jr.; Schlesinger, H. I. (1947). "Lithium Aluminum Hydride, Aluminum Hydride and Lithium Gallium Hydride, and Some of their Applications in Organic and Inorganic Chemistry". Journal of the American Chemical Society. 69 (5). ss. 1199-1203. doi:10.1021/ja01197a061.
- ^ US patent 6228338, Petrie, M. A.; Bottaro, J. C.; Schmitt, R. J.; Penwell, P. E.; Bomberger, D. C., "Preparation of Aluminum Hydride Polymorphs, Particularly Stabilized α-AlH3", Veriliş tarihi: 2001-05-08
- ^ Schmidt, D. L.; Roberts, C. B.; Reigler, P. F.; Lemanski, M. F. Jr.; Schram, E. P. (1973). "Aluminum Trihydride-Diethyl Etherate: (Etherated Alane)". Inorganic Syntheses. Inorganic Syntheses. Cilt 14. ss. 47-52. doi:10.1002/9780470132456.ch10. ISBN 9780470132456.
- ^ Alpatova, N. M.; Dymova, T. N.; Kessler, Yu. M.; Osipov, O. R. (1968). "Physicochemical Properties and Structure of Complex Compounds of Aluminium Hydride". Russian Chemical Reviews. 37 (2). ss. 99-114. Bibcode:1968RuCRv..37...99A. doi:10.1070/RC1968v037n02ABEH001617.
- ^ Semenenko, K. N.; Bulychev, B. M.; Shevlyagina, E. A. (1966). "Aluminium Hydride". Russian Chemical Reviews. 35 (9). ss. 649-658. Bibcode:1966RuCRv..35..649S. doi:10.1070/RC1966v035n09ABEH001513.
- ^ Osipov, O. R.; Alpatova, N. M.; Kessler, Yu. M. (1966). "none". Elektrokhimiya. Cilt 2. s. 984.
- ^ a b Zidan, R.; Garcia-Diaz, B. L.; Fewox, C. S.; Stowe, A. C.; Gray, J. R.; Harter, A. G. (2009). "Aluminium hydride: a reversible material for hydrogen storage". ChemComm, 25. ss. 3717-3719. doi:10.1039/B901878F.
- ^ a b Martinez-Rodriguez, M. J.; Garcia-Diaz, B. L.; Teprovich, J. A.; Knight, D. A.; Zidan, R. (2012). "Advances in the electrochemical regeneration of aluminum hydride". Applied Physics A: Materials Science & Processing. 106 (25). ss. 545-550. Bibcode:2012ApPhA.106..545M. doi:10.1007/s00339-011-6647-y.
- ^ DE patent 1141623, Clasen, H., "Verfahren zur Herstellung von Aluminiumhydrid bzw. aluminiumwasserstoffreicher komplexer Hydride", Veriliş tarihi: 1962-12-27, Veren: Metallgesellschaft
- ^ US patent 8470156, Zidan, R., "Electrochemical process and production of novel complex hydrides", Veriliş tarihi: 2013-06-25, Veren: Savannah River Nuclear Solutions, LLC
- ^ Saitoh, H; Sakurai, Y; Machida, A; Katayama, Y; Aoki, K (2010). "In situX-ray diffraction measurement of the hydrogenation and dehydrogenation of aluminum and characterization of the recovered AlH3". Journal of Physics: Conference Series. Cilt 215. s. 012127. Bibcode:2010JPhCS.215a2127S. doi:10.1088/1742-6596/215/1/012127. ISSN 1742-6596.
- ^ a b Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2. bas.). Butterworth-Heinemann. ISBN 0080379419.
- ^ Atwood, J. L.; Bennett, F. R.; Elms, F. M.; Jones, C.; Raston, C. L.; Robinson, K. D. (1991). "Tertiary Amine Stabilized Dialane". Journal of the American Chemical Society. 113 (21). ss. 8183-8185. doi:10.1021/ja00021a063.
- ^ Yun, J.-H.; Kim, B.-Y.; Rhee, S.-W. (1998). "Metal-Organic Chemical Vapor Deposition of Aluminum from Dimethylethylamine Alane". Thin Solid Films. 312 (1-2). ss. 259-263. Bibcode:1998TSF...312..259Y. doi:10.1016/S0040-6090(97)00333-7.
- ^ Galatsis, P. (2001). "Diisobutylaluminum Hydride". Encyclopedia of Reagents for Organic Synthesis. Encyclopedia of Reagents for Organic Synthesis. doi:10.1002/047084289X.rd245. ISBN 978-0-470-84289-8.
- ^ Ayres, D. C.; Sawdaye, R. (1967). "The Stereoselective Reduction of Ketones by Aluminium Hydride". Journal of the Chemical Society B. Cilt 1967. ss. 581-583. doi:10.1039/J29670000581.
- ^ Corey, E. J.; Cane, D. E. (1971). "Controlled Hydroxymethylation of Ketones". Journal of Organic Chemistry. 36 (20). ss. 3070-3070. doi:10.1021/jo00819a047.
- ^ Jorgenson, Margaret J. (Temmuz 1962). "Selective reductions with aluminum hydride". Tetrahedron Letters. 3 (13). ss. 559-562. doi:10.1016/S0040-4039(00)76929-2.
- ^ Takano, S.; Akiyama, M.; Sato, S.; Ogasawara, K. (1983). "A Facile Cleavage of Benzylidene Acetals with Diisobutylaluminum Hydride" (pdf). Chemistry Letters. 12 (10). ss. 1593-1596. doi:10.1246/cl.1983.1593.[ölü/kırık bağlantı]
- ^ Richter, W. J. (1981). "Asymmetric Synthesis at Prochiral Centers: Substituted 1,3-Dioxolanes". Journal of Organic Chemistry. 46 (25). ss. 5119-5124. doi:10.1021/jo00338a011.
- ^ Maruoka, K.; Saito, S.; Ooi, T.; Yamamoto, H. (1991). "Selective Reduction of Methylenecycloalkane Oxides with 4-Substituted Diisobutylaluminum 2,6-Di-tert-butylphenoxides". Synlett. 1991 (4). ss. 255-256. doi:10.1055/s-1991-20698.
- ^ Claesson, A.; Olsson, L.-I. (1979). "Allenes and Acetylenes. 22. Mechanistic Aspects of the Allene-Forming Reductions (SN2' Reaction) of Chiral Propargylic Derivatives with Hydride Reagents". Journal of the American Chemical Society. 101 (24). ss. 7302-7311. doi:10.1021/ja00518a028.
- ^ Corey, E. J.; Katzenellenbogen, J. A.; Posner, G. H. (1967). "New Stereospecific Synthesis of Trisubstituted Olefins. Stereospecific Synthesis of Farnesol". Journal of the American Chemical Society. 89 (16). ss. 4245-4247. doi:10.1021/ja00992a065.
- ^ Sato, F.; Sato, S.; Kodama, H.; Sato, M. (1977). "Reactions of Lithium Aluminum Hydride or Alane with Olefins Catalyzed by Titanium Tetrachloride or Zirconium Tetrachloride. A Convenient Route to Alkanes, 1-Haloalkanes and Terminal Alcohols from Alkenes". Journal of Organometallic Chemistry. 142 (1). ss. 71-79. doi:10.1016/S0022-328X(00)91817-5.
- ^ a b Graetz, J.; Reilly, J.; Sandrock, G.; Johnson, J.; Zhou, W. M.; Wegrzyn, J. (2006). "Aluminum Hydride, A1H3, As a Hydrogen Storage Compound". doi:10.2172/899889.
Dış bağlantılar[değiştir | kaynağı değiştir]
- EnvironmentalChemistry.com sitesinde Alüminyum Hidrit Kimyasal Veritabanı
- Brookhaven National Laboratory sitesinde Hidrojen Depolama
- WebElements sitesinde Alüminyum Trihidrit 30 Kasım 2016 tarihinde Wayback Machine sitesinde arşivlendi.
Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? Nedir? :Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? ile ilgili Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? burada bulabilirsiniz. Detaylar için sitemizi geziniz Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? Ne Demektir? Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? Açıklaması Nedir? Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? Cevabı Nedir? Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? Kelimesinin Anlamı? Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? konusu Nedir Ne, yaşantımızda sık kullanılan kelimelerden birisi olarak karşımıza çıkar. Hem sosyal medyada hem de gündelik yaşantıda kullanılan ne kelimesi, uzun yıllardan beri dilimizdedir. Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? Türk Dil Kurumu na (TDK) göre farklı anlamları olan ne kelimesi, Türkçe de tek başına ya da çeşitli cümleler eşliğinde kullanılabilir. Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? Ne kelimesi ne demek, TDK ya göre anlamı nedir sorularının cevabını arayanlar için bildiris.com doğru adres! Peki, ne kelimesi ne demek, TDK ye göre anlamı nedir? Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? Ne kelimesinin kökeni ne, ne kelimesinin kaç anlamı var? Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? İşte TDK bilgileri ile merak edilenler
Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? Açıklaması? :Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? Açıklama Bir Terim Kavram Ya Da Başka Dilsel Olgunun Daha İyi Anlaşılması İçin Yapılan Ek Bilgidir.Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? Söz Konusu Bilgi Açıklanacak Sözcükten Daha Uzun Olur Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? Açıklama İle İlgili Durumun Kanıtı Şu Şekilde Doğrulanabilir Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? Bir Sözlükteki Tanım İlgili Sözcük Yerine Kullanılabilirse, Bu Bir Açıklamadır. Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? Yani Aynı Bağlam İçinde Hem Sözcük Hem De Tanım Kullanılırsa Ve Anlamsal Açıdan Bir Sorun Oluşturmuyorsa Bu Bir Açıklamadır.
Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? Gerçek mi? :Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? ile ilgili Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? burada bulabilirsiniz. Detaylar için sitemizi geziniz Gerçek anlam Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? sözcüklerin birincil anlamı ile (varsa) bu anlamla doğrudan ilişkili olan anlamlarıdır. Gerçek anlam, temel anlam ile yan anlamların bileşkesidir. Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? Bir sözcüğün mecaz olmayan tüm anlamlarını kapsar.
Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? Hakkında? :Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? ile ilgili Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? burada bulabilirsiniz. Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? Detaylar için sitemizi geziniz Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? Bu sayfada Hakkında nedir Hakkında ne demek Hakkında ile ilgili sözler cümleler bulmaca kısaca Hakkında anlamı tanımı açılımı Hakkında hakkında bilgiler Alüminyum hidrit nedir?, Alüminyum hidrit anlamı nedir?, Alüminyum hidrit ne demektir? resimleri Hakkında sözleri yazıları kelimesinin sözlük anlamı nedir almanca ingilizce türkçe çevirisini bulabilirsiniz
Fosfatlı Nedir?, Topsuz Nedir?, Sovyetler Birliği bayrağı Anlamı Nedir, Sovyetler Birliği bayrağı Nasıl Oluştu, Sovyetler Birliği bayrağı Tarihi, Sovyetler Birliği bayrağı Renkleri, Sovyetler Birliği bayrağı Tasarımı, Aslan Sezgin Kimdir?, Topraksız Nedir?, Şener Pul Kimdir?, Topraksı Nedir?, Serap Çakır Kimdir?, Selma Karaman Kimdir?, Formaliteci Nedir?, Yavuz Tellioğlu Kimdir?, Toprakçıl Nedir?, Forgetful Nedir?, Sırbistan-Karadağ bayrağı Anlamı Nedir, Sırbistan-Karadağ bayrağı Nasıl Oluştu, Sırbistan-Karadağ bayrağı Tarihi, Sırbistan-Karadağ bayrağı Renkleri, Sırbistan-Karadağ bayrağı Tasarımı, Toprak Rengi Nedir?, For Nedir?, İsmail Aybars Aksoy Kimdir?, Nail Çiler Kimdir?, Toprak Altı Nedir?, Fonolojik Nedir?, Bekir Sıtkı Tarım Kimdir?, İhsan Sarıyar Kimdir?, Topolojik Nedir?, Hasan Bitmez Kimdir?, Topoğrafik Nedir?, Sancak-ı Şerif Anlamı Nedir, Sancak-ı Şerif Nasıl Oluştu, Sancak-ı Şerif Tarihi, Sancak-ı Şerif Renkleri, Sancak-ı Şerif Tasarımı, Lütfi İlteriş Öney Kimdir?, Ufuk Değerliyurt Kimdir?, Folklorik Nedir?, Rana Berk Kimdir?, Toplum Dışı Nedir?, Fokurdak Nedir?, Toplum Bilimsel Nedir?, Fodulca Nedir?, Ayla Bedirhan Çelik Kimdir?, Harun Özgür Yıldızlı Kimdir?, Samara bayrağı Anlamı Nedir, Samara bayrağı Nasıl Oluştu, Samara bayrağı Tarihi, Samara bayrağı Renkleri, Samara bayrağı Tasarımı, Figen Yıldırım Kimdir?, Flüoresan Nedir?, Ayhan Özçelik Kimdir?, Toplanık Nedir?, İzzet Kaplan Kimdir?, Mühip Kanko Kimdir?, Prensin Bayrağı Anlamı Nedir, Prensin Bayrağı Nasıl Oluştu, Prensin Bayrağı Tarihi, Prensin Bayrağı Renkleri, Prensin Bayrağı Tasarımı, Recep Bozdemir Kimdir?, Ali Topçu Kimdir?, Toparlakça Nedir?, Hurşit Çetin Kimdir?, Fadik Temizyürek Kimdir?, Toparlağımsı Nedir?, Toparlacık Nedir?, Osmanlı bayrağı Anlamı Nedir, Osmanlı bayrağı Nasıl Oluştu, Osmanlı bayrağı Tarihi, Osmanlı bayrağı Renkleri, Osmanlı bayrağı Tasarımı, Ülkü Doğan Kimdir?, Mehmet Akif Perker Kimdir?, Necmi Özgül Kimdir?, Top Sakallı Nedir?, Hasan Daşkın Kimdir?, Hasan Memişoğlu Kimdir?, Nazi Almanyası bayrağı Anlamı Nedir, Nazi Almanyası bayrağı Nasıl Oluştu, Nazi Almanyası bayrağı Tarihi, Nazi Almanyası bayrağı Renkleri, Nazi Almanyası bayrağı Tasarımı, Fitopatolojik Nedir?, Öztürk Keskin Kimdir?, Şeref Baran Genç Kimdir?, Tonla Nedir?, Nuran Ergen Kılıç Kimdir?, Fitne Kumkuması Nedir?, Filiz Orman Akın Kimdir?, Tombulca Nedir?, Fitne Fücur Nedir?, Zürriyetsiz İsminin Anlamı Nedir?, Fitilsiz Nedir?, Natalia Cumhuriyeti Bayrağı Anlamı Nedir, Natalia Cumhuriyeti Bayrağı Nasıl Oluştu, Natalia Cumhuriyeti Bayrağı Tarihi, Natalia Cumhuriyeti Bayrağı Renkleri, Natalia Cumhuriyeti Bayrağı Tasarımı, Zürriyetli İsminin Anlamı Nedir?, Mustafa Süleyman Kurtar Kimdir?, Züppe İsminin Anlamı Nedir?, Fitilci Nedir?, Dağıstan Budak Kimdir?, Yrd Doç Dr Bilge Gökçen Röhlig Kimdir? Yrd Doç Dr Bilge Gökçen Röhlig Nereli Yrd Doç Dr Bilge Gökçen Röhlig Kaç Yaşında?, Zümrüdi İsminin Anlamı Nedir?, Tolgasız Nedir?, Fitçi Nedir?, Hatice Gül Bingöl Kimdir?, Gökhan Baylan Kimdir?, Zülüflü İsminin Anlamı Nedir?, Tolgalı Nedir?, Fişlik Nedir?, Kampuçya Halk Cumhuriyeti bayrağı Anlamı Nedir, Kampuçya Halk Cumhuriyeti bayrağı Nasıl Oluştu, Kampuçya Halk Cumhuriyeti bayrağı Tarihi, Kampuçya Halk Cumhuriyeti bayrağı Renkleri, Kampuçya Halk Cumhuriyeti bayrağı Tasarımı, Toleranssız Nedir?, Züllü İsminin Anlamı Nedir?, Fişli Nedir?, Fişeksiz Nedir?, Zülcelâl İsminin Anlamı Nedir?, Sözdar Akdoğan Kimdir?, Murat Turna Kimdir?, Fahri Özkan Kimdir?, Zührevi İsminin Anlamı Nedir?, Fişekli Nedir?, Züğürt İsminin Anlamı Nedir?, İzmir bayrağı Anlamı Nedir, İzmir bayrağı Nasıl Oluştu, İzmir bayrağı Tarihi, İzmir bayrağı Renkleri, İzmir bayrağı Tasarımı, Filiz Çelik Kimdir?, Toksikolojik Nedir?,